Conoce leyendo este artículo qué es un electrolito y qué tipos existen, además qué es la electrolisis y cuáles sons sus principales aplicaciones.
Qué es un electrolito
Los electrolitos son sustancias compuestas de iones libres, que permiten o hacen que se comporte como un conductor eléctrico.
Otra definición común indica que sustancias que al disolverse en agua, dan lugar a la formación de iones (partículas cargadas de electricidad).
Ya que se encuentran también iones en la disolución, los electrolitos son conocidos por el nombre de soluciones iónicas.
Un electrolito, por lo tanto, viene a ser lo que llamamos conductor iónico, también conocido como conductor de segunda especie.
Los electrolitos pueden conducir corriente eléctrica, a causa de tener presentes iones positivos y negativos generados en la solución, derivada de la disociación y de ionización del electrolito.
En el cuerpo humano existen electrolitos necesarios para regular nuestro pH sanguíneo, para la hidratación corporal y el funcionamiento de los músculos.
Algunos iones que son “primarios” o principales en los electrolitos de la fisiología son, el calcio, el potasio, el magnesio y el sodio.
Los electrolitos pueden ser débiles o fuertes, y esto lo determina si están parcial o totalmente ionizados o disociados en medio acuoso.
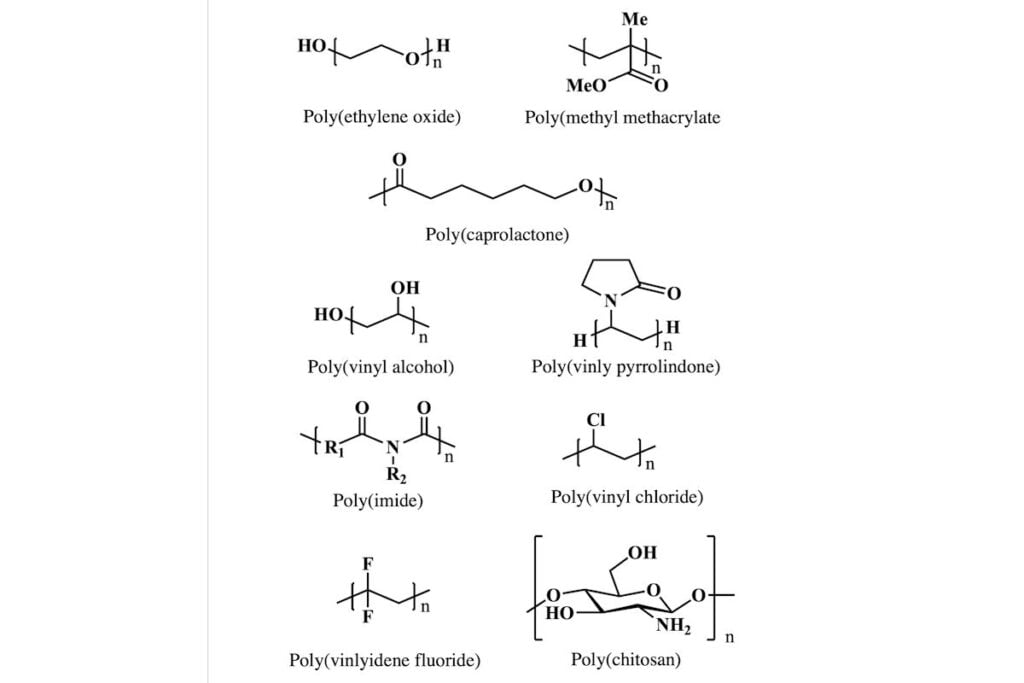
Electrolito fuerte
El término electrolito fuerte hace referencia a una sustancia que al disolverse en agua, provoca la formación de iones con una reacción de disolución irreversible.
Este tipo de electrolitos se ionizan completamente, es decir, al 100%.
Como ejemplos de electrolitos fuertes tenemos los ácidos clorhídrico (HCl), sulfúrico (H2SO4) y nítrico (HNO3), también todos los hidróxidos (excepto el hidróxido de amonio NH4OH) y la mayoría de las sales.
Electrolito débil
Un electrolito débil es una sustancia que al disolverse en agua, produce iones parcialmete, con reacciones reversibles.
Debido a que los electrolitos débiles se ionizan de forma parcial, su porcentaje de ionización está entre 1 y 10%.
Entre los electrolitos débiles se encuentran los ácidos acético, benzoico, fórmico, carbónico, fosfórico, sulfuroso, y también la Dimetilamina y la Etilamina.
Tipos de electrolitos
- Soluciones electrolíticas: ejemplo, ácido clorhídrico y ácido sulfúrico.
- Electrolitos sólidos: ejemplo, β- alúmina, forma alotrópica de óxido de aluminio.
- Sólidos iónicos: ejemplo, cloruro de sodio, yoduro de plata y fluoruro de calcio.
- Sales fundidas: ejemplo, nitratos alcalinos.
- Electrolito fuerte: solución con alto porcentaje del soluto que se disocia para crear iones libres
- Electrolito débil: la mayor parte del soluto no consigue disociarse
Aplicaciones de los electrolitos
Los electrolitos pueden ser usados como componentes de celdas electroquímicas para transportar carga eléctrica de un electrodo a otro.
Además, se usan dentro de condensadores particulares que llevan por nombre condensadores electrolíticos.
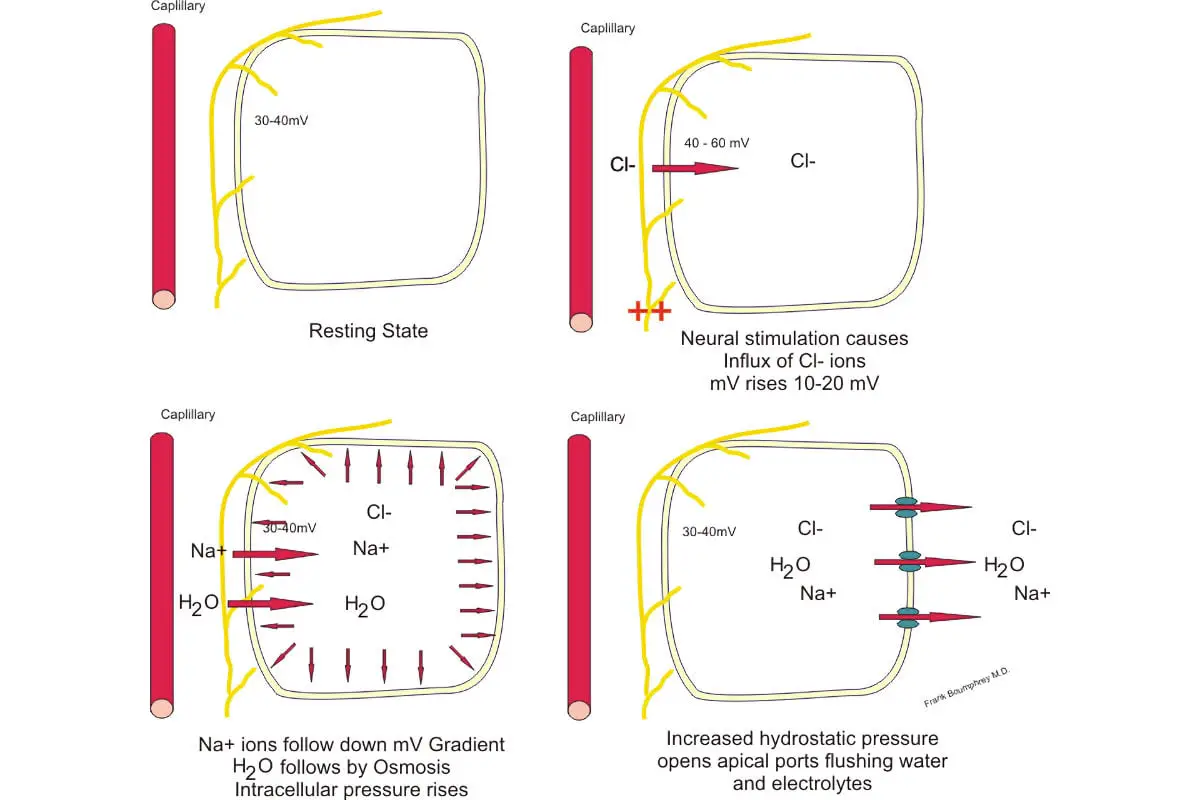
En el campo de la biología, los electrolitos son aplicables y esenciales para algunos procesos biológicos, como por ejemplo la bomba de sodio y potasio.
En la sangre, específicamente en el plasma, están presentes sodio, potasio, fosfato, magnesio, hierro, calcio y otros elementos clave.
Electrolisis
La electrolisis es un fenómeno que consiste en la descomposición de electrolitos por medio de la corriente eléctrica. Dicha descomposición se realiza en las cubas electrolíticas o en los voltámetros.
Las aplicaciones de la electrolisis son numerosas debido a que este fenómeno permite la preparación o la purificación de numerosos elementos químicos como el hidrógeno, flúor y cloro.
Además, metales como el cobre, el zinc y el mercurio se obtienen por electrolisis, tras la disolución de sus minerales en ácido súlfurico. También, el sodio y el magnesio se obtienen por la electrolisis de sus cloruros, por su parte el aluminio se obtiene a partir de su óxido.
Asimismo, la electrolisis es usada para recubrir objetos metálicos con una capa delgada de otro metal, para mejorar su aspecto y características. Estas son las llamadas aplicaciones galvanotécnicas.